
主编按语·熊建萍教授
在临床真实世界,对医师最有启发意义的就是病例分享,面对千变万化的病人,如果能够抓住临床诊治的核心,万变不离其宗,病人是否获得良好的长期生存,往往就在医师的一个关键选择,因此作为肿瘤临床医师,不断学习最新知识,不断总结临床经验,用心细致分析病情变化极为重要。我们消化肿瘤团队病床数达到200张,每年收治消化肿瘤1500人次,为我省消化肿瘤病人解除病痛努力拚博,获得广泛好评。本期病例分享,青年医师不约而同选择了自己行医历程中印象深刻的,给病人带来较好疗效的成功病例,我们看到从掌握基础知识出发,推理临床实践和应用,在多线治疗病情仍然进展危害病人生命时,尽可能根据精准医学指导,选择最新的免疫治疗或靶向治疗,使病人峰回路转柳暗花明重获新生。
本期执行主编

熊建萍教授
南昌大学第一附属医院肿瘤科主任医师、二级教授、博士生导师
江西省政府特殊津贴获得专家
中华医学会肿瘤分会委员
中国女医师协会临床肿瘤分会常委
中国抗癌协会支持治疗专业委员会常委/化疗专业委员会常委/肺癌专委会常委
中国肿瘤临床学会理事
第四期
熊建萍教授力荐:《FDFT1/FGFR2重排:胆管细胞癌中新发现的FGFR2变异且对安罗替尼治疗敏感》

项晓军主任
南昌大学第一附属医院肿瘤科主任医师、博士生导师
CSCO结直肠癌专委会委员
CSCO胰腺癌专委会青年委员
中国抗癌协会肿瘤支持治疗专委会青年委员
北京癌症防治学会胃癌防治专委会常委

邓军
南昌大学第一附属医院肿瘤中心医师、副主任医师、博士,硕士研究生导师
江西省腹部肿瘤个体化诊治重点实验室常务副主任
2020年江西省主要学科学术和技术带头人(青年)
以第一作者或共同通讯作者发表SCI论文10余篇,累积IF50分
留学归国人员,主持国家自然科学基金1项,其余省级项目6项
2018年江西省杰出青年基金获得者
正文如下
摘要
既往研究报道,临床上有10%-16%的晚期胆管细胞癌患者会出现FGFR2融合或重排,对FGFR2特异性抑制剂(TKIs)治疗有效。本文报告1例晚期胆管癌患者,在经过一线标准化疗后,因无法耐受化疗相关不良反应,经基因检测发现了一种全新的变异--FDFT1/FGFR2重排,但由于FGFR2特异性抑制剂在中国可及性差,价格昂贵,导致很多晚期胆管癌患者仍无法获得精准靶向治疗。Anlotinib是中国自主研发的一种新型小分子多靶点酪氨酸激酶抑制剂,能广泛抑制FGFR在内的多个靶点,有效减少肿瘤血管生成和抑制肿瘤细胞增殖,达到抗肿瘤目的。我们尝试用安罗替尼治疗该患者,有趣的是,该患者经安罗替尼治疗后肿瘤持续缩小,不良反应轻,提示安罗替尼治疗对于FDFT1/FGFR重排可能有效,将来可能为这部分患者提供新的治疗选择。
前言
胆管细胞癌(CCA)是仅次于肝细胞癌(HCC)的第二大原发性肝恶性肿瘤,占原发性肝肿瘤的15%和消化系统肿瘤的3%[1],其发病率及死亡率在全球大部分国家/地区呈不同程度的上升趋势。手术切除仍是目前胆管细胞癌的主要治疗手段,但只有大约三分之一的新诊断患者符合手术条件,且术后的复发率或转移率高达70%,5年生存率仅为5%-10%[2]。
研究报道,在胆管细胞癌中,约有10-16%的患者会出现FGFR2融合或重排[3-4],一些FGFR2的选择性和非选择性抑制剂正在进行临床试验[5,6]。目前批准用于晚期胆管癌的的FGFR2抑制剂在中国可及性差,价格昂贵,导致很多晚期胆管癌患者仍无法获得精准靶向治疗。
安罗替尼(Anlotinib)能有效抑制包含FGFR2在内的多个靶点及其介导的通路,从而抑制肿瘤血管生成和肿瘤增殖生长[7]。安罗替尼已被批准用于晚期非小细胞肺癌(NSCLC)、晚期甲状腺髓样癌、转移性肾细胞癌癌,和软组织肉瘤等[8-12]。在这篇文章中,我们首次发现一例FDFT1/FGFR2重排的晚期胆管癌患者,经一线标准化疗后,使用酪氨酸激酶抑制剂安罗替尼治疗后有效。
病例介绍
患者中年女性,45岁,2020年4月6日因上腹部疼痛15天首次就诊于南昌大学第一附属医院。入院后2020年4月7日CT检查提示肝内多发占位性病变并肝门部肿大淋巴结,头颅磁共振及骨扫描未见明显异常。2020年4月8日,B超引导下经皮肤肝脏穿刺活检病理提示胆管细胞癌,免疫组化提示:CK19(+),Hep(-),CK7(+),CK20(-),Villin(+),CDX2(+),Gly(-),HSP70(-),CA125(-),CD34(-),Ki-67(40%+),TTF1(-)(Fig1),患者诊断为IV期胆管细胞癌。肝功能分级(Child-Pugh分级标准)A级。饮酒史20年余,否认吸烟。既往乙肝小三阳(乙型肝炎表面抗原、e抗体及核心抗体阳性)5年余,未接受抗病毒治疗。家族史无特殊。

2020年4月17日至2020年8月12日,患者接受了一线6个疗程奥沙利铂(100mg/m2,d1)联合吉西他滨(1000mg/m2,d1和d8)静脉化疗,每3周1次,同时长期口服恩替卡韦胶囊抗乙肝病毒治疗。4程、6程化疗后患者分别行CT复查提示肝内病灶较前减小(Fig2)。
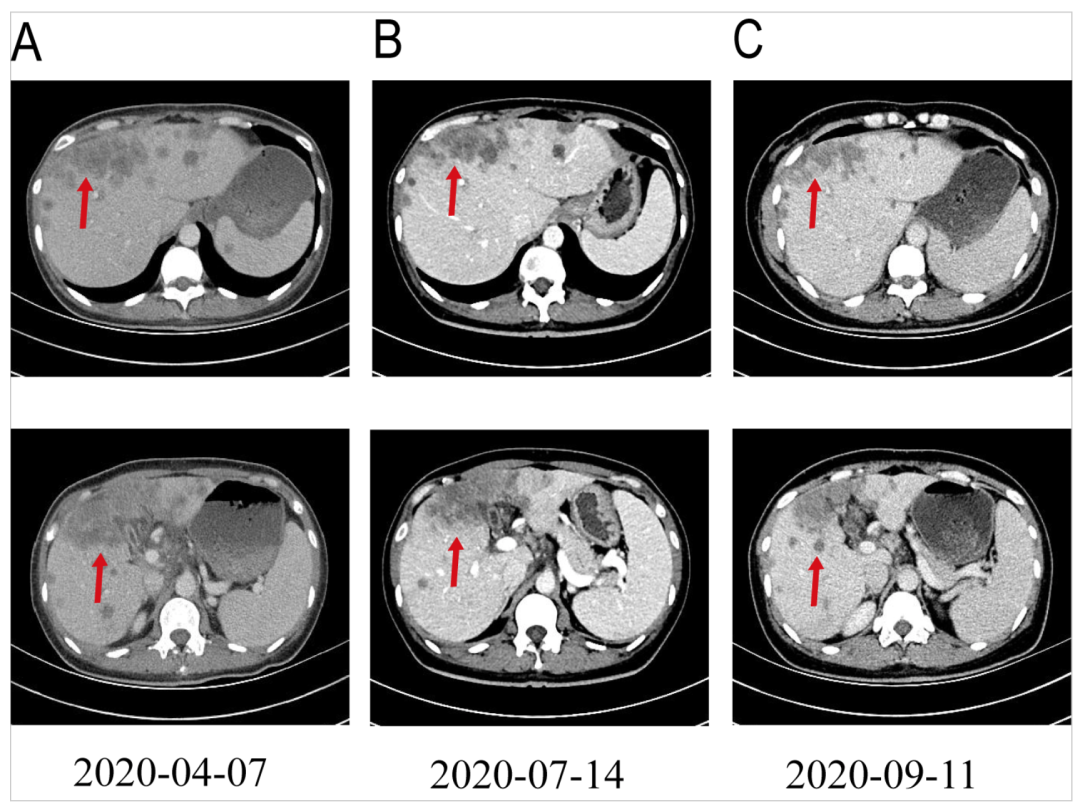
患者在化疗期间出现III度血小板减少及白细胞减少的血液系统毒性,并出现II度恶心呕吐、食欲减退的治疗相关胃肠道反应,拒绝继续化疗。行NGS基因检测发现患者存在FDFT1/FGFR2基因重排(Fig3),并再次行免疫组化提示:FGFR2蛋白高表达(Fig4)。
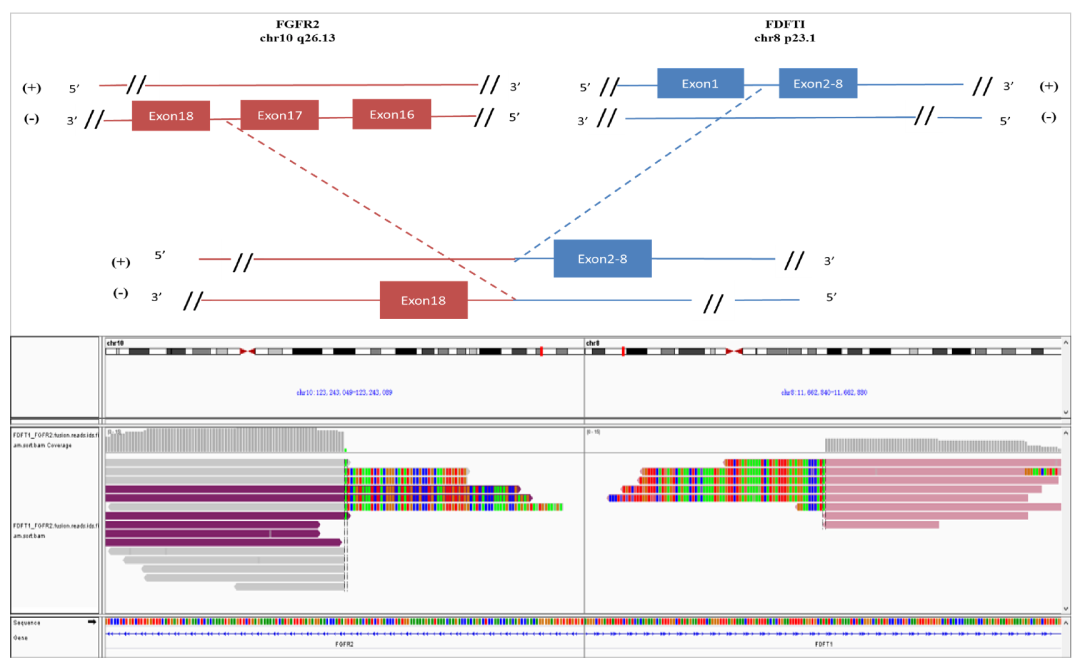
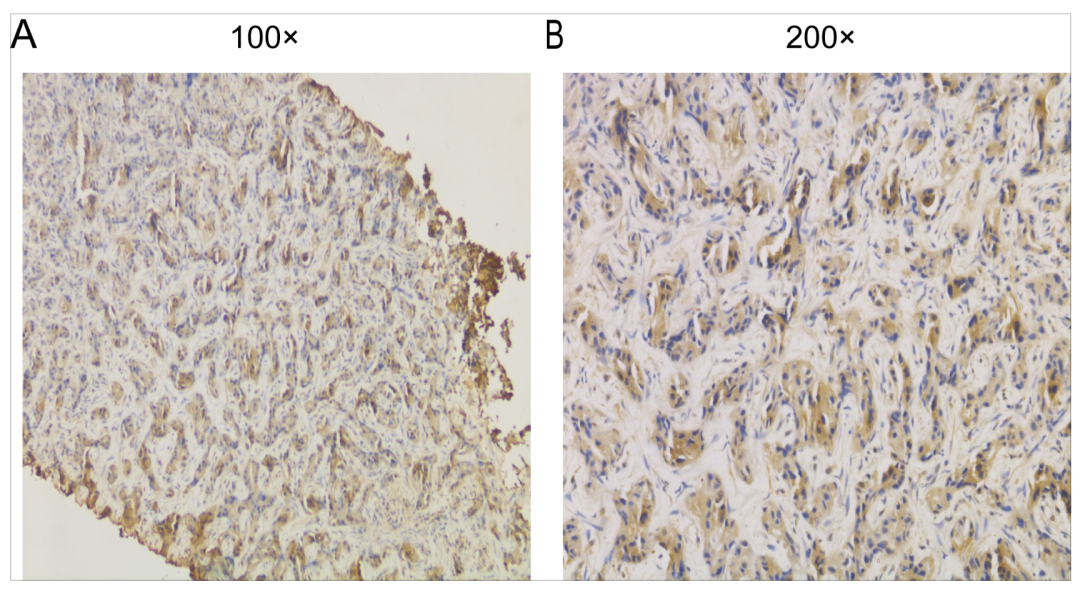
目前,已获FDA批准用于治疗FGFR2融合或重排的转移性胆管癌的药物有Futibatinib(TAS-120)和Pemigatinib等,但由于国内该类抑制剂的可及性差,价格昂贵,患者接受不了该药物治疗。经过充分沟通,我们为患者选择口服安罗替尼靶向治疗。患者自2020年9月15日开始接受安罗替尼(8mg,d1-14,q3w)治疗,口服安罗替尼4程、8程后复查CT提示肝内病灶较前持续缩小(Fig5),根据评价标准,患者疗效评价达部分缓解(PR)。安罗替尼治疗期间患者耐受情况良好,仅出现1级口腔黏膜炎、2级手足综合征及1级血清甘油三酯升高(按标准)。直到最近一次随访,患者一般情况良好,影像学复查提示肿瘤稳定。
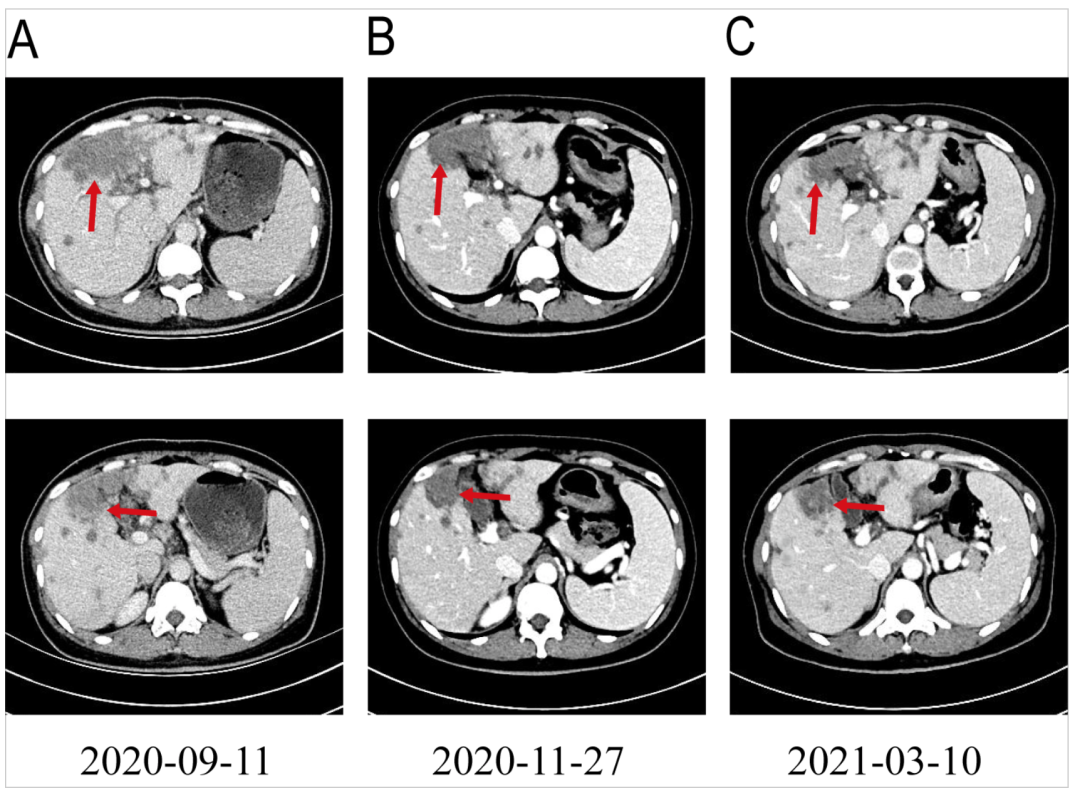
讨论
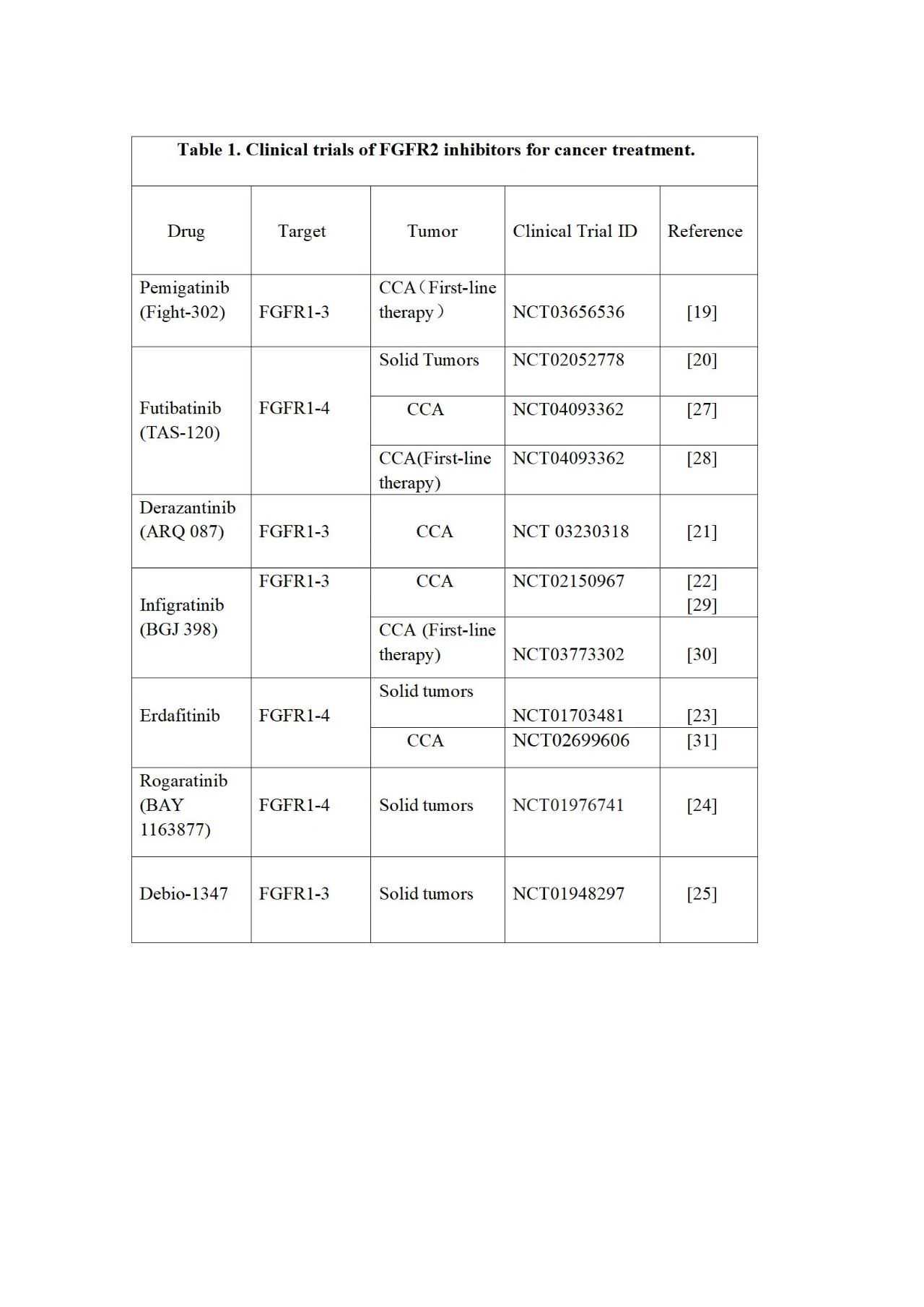
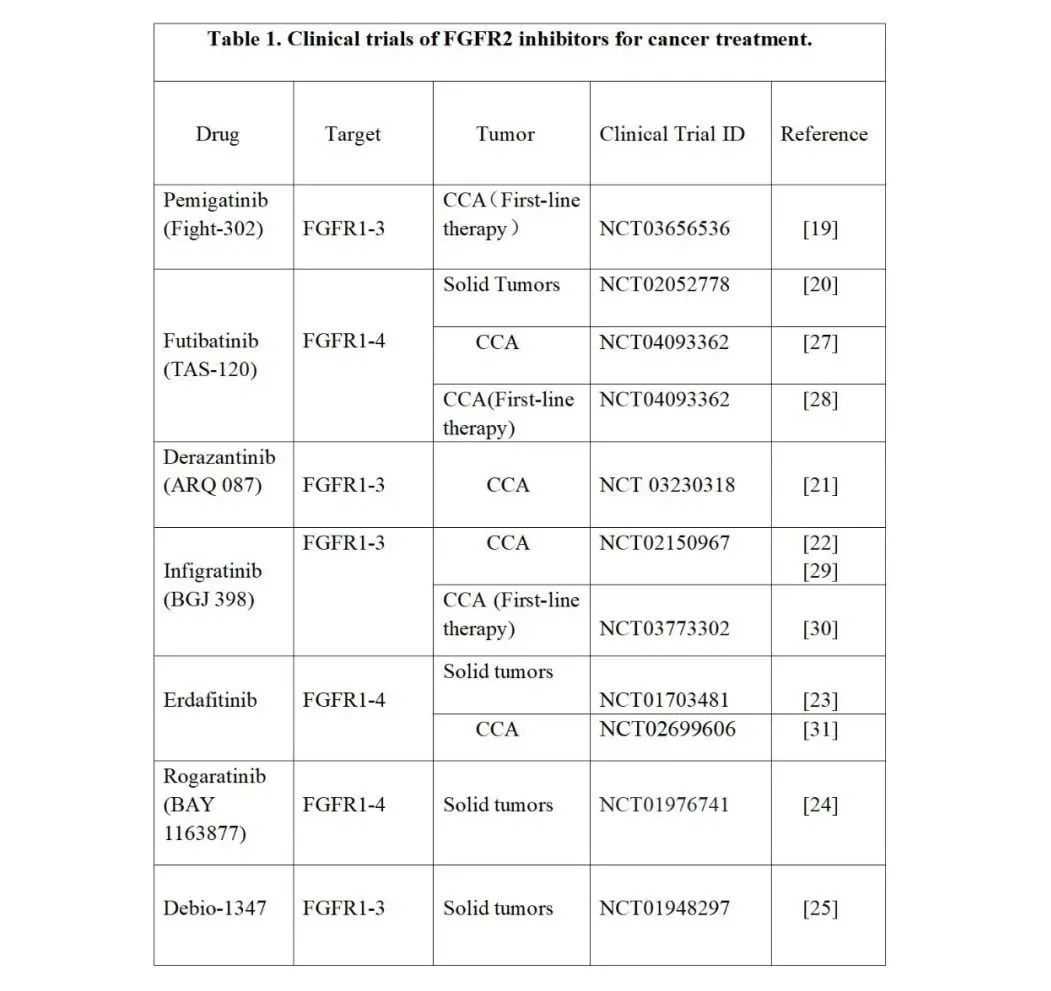
考虑到目前晚期胆管癌一线化疗效益相对较小,缺乏有效的二线治疗方案,且目前胆管癌患者免疫治疗效果不佳,因此迫切需要新的治疗方法。目前,在晚期胆管癌中已经发现了一些新靶点,如FGFR、IDH1/2等,使得靶向治疗胆管癌成为一种可行的手段[13-15]。近年来,FGFR抑制剂在胆管癌领域大放异彩。Pemigatinib是一种靶向FGFR1/2/3的强效选择性口服激酶抑制剂,通过阻滞FGFR及其下游信号通路而发挥抗肿瘤作用[16]。根据临床研究结果,FDA已批准Pemigatinib用于治疗FGFR2融合或重排的转移性胆管癌患者[17]。另外,FOENIX-CCA2研究的中期结果显示:FGFR1-4小分子抑制剂--Futibatinib(TAS-120),在FGFR2融合或重排的转移性胆管癌患者的治疗中表现不凡[18][27]。2021年4月3日,FDA已授予Futibatinib突破性药物资格。目前,有多项针对胆管癌的FGFR抑制剂正在进行临床研究,我们列举了其中部分(Table1)[19-25][28-31]。
本文中报告的患者,在经过一线标准化疗后,因无法耐受化疗相关不良反应,经基因检测发现患者出现了一种全新的变异--FDFT1/FGFR2重排,但由于FGFR2特异性抑制剂在中国可及性差,很多患者无法使用上该类药物,失去靶向治疗机会。研究表明,Anlotinib是中国自主研发的一种新型小分子多靶点酪氨酸激酶抑制剂,能广泛抑制FGFR(FGFR1-4)、VEGFR(VEGFR1-3),PDGFR(PDGFR-a和PDGFR-b)和c-kit等多个靶点,有效减少肿瘤血管生成和抑制肿瘤细胞增殖,达到抗肿瘤目的[26]。我们尝试用安罗替尼继续治疗,有趣的是,该患者经安罗替尼治疗后肿瘤持续缩小,提示安罗替尼治疗对于FDFT1/FGFR2重排可能有效,将来可能为这部分患者提供新的治疗选择。
项晓军、熊建萍点评
目前针对胆管癌的治疗方式并不多,一线的治疗方式多是采用化疗的方法,但效果并不是十分的理想,而且还经常会发生耐药性。在胆管癌患者中,FGFR融合突变比较突出。研究数据显示,胆管癌患者中有13%-20%的患者携带FGFR2融合突变,这些患者很有可能适合使用FGFR抑制剂。2020年4月FDA已批准Pemigatinib用于治疗FGFR2融合或重排的晚期胆管癌患者。今年4月初,基于FOENIX-CCA2中期结果,Futibatinib也被FDA批准。我们在该病例中检测到FDFT1/FGFR2重排这一新变异,但由于当时国内FGFR2特异性抑制剂可及性差,我们选择安罗替尼靶向治疗。安罗替尼能广泛抑制FGFR2在内的多个靶点,患者经治疗后疗效较好,不良反应轻,为晚期胆管癌患者的靶向治疗提供新选择。
参考文献
1.Bertuccio,P.,etal.,Globaltre,2019.71(1):
2.Rizvi,S.,etal.,,2018.15(2):
3.Graham,,etal.,Fibroblastgrow,2014.45(8):
4.Goyal,L.,etal.,PolyclonalSecondaryFGFR2MutationsDriveAcquiredResistancetoFGF,2017.7(3):
5.Lee,,etal.,TargetingtheFibroblastGrowthFactorReceptor(FGFR)inAdvancedCholangiocarcinoma:(Basel),2021.13(7).
6.Krook,,etal.,EfficacyofFGFRInhibitorsandCombinatio,2020.19(3):
7.Shen,G.,etal.,Anlotinib:an,2018.11(1):
8.Sun,Y.,etal.,Safety,pharmacokinetics,andantitumorpropertiesofanlotinib,anoralmulti-targettyrosinekinaseinhibitor,,2016.9(1):
9.Han,B.,etal.,EffectofAnlotinibasaThird-LineorFurtherTreatmentonOverallSurvivalofPatientsWithAdvancedNon-SmallCellLungCancer:,2018.4(11):
10.Zhou,,etal.,AnlotinibVersusSunitinibasFirst-LineTreatmentforMetastaticRenalCellCarcinoma:,2019.24(8):
11.Sun,Y.,etal.,AnlotinibfortheTreatment,2018.28(11):
12.Chi,Y.,etal.,SafetyandEfficacyofAnlotinib,aMultikinaseAngiogenesisInhibitor,,2018.24(21):
13.Farshidfar,F.,etal.,IntegrativeGenomicAnalysisof,2017.18(11):
14.Katoh,,FGFreceptors:,2014.34(2):
15.Lamarca,A.,etal.,Moleculartargetedtherapies:Readyfor"primetime",2020.73(1):
16.Liu,,etal.,INCB054828(pemigatinib),apotentandselectiveinhibitoroffibroblastgrowthfactorreceptors1,2,and3,,2020.15(4):
17.Abou-Alfa,,etal.,Pemigatinibforpreviouslytreated,locallyadvancedormetastaticcholangiocarcinoma:amulticentre,open-label,,2020.21(5):
18.Sootome,H.,etal.,FutibatinibIsaNovelIrreversibleFGFR1-4InhibitorT,2020.80(22):
19.Bekaii-Saab,,etal.,FIGHT-302:first-linepemigatinibvsgemcitabinepl,2020.16(30):
20.Bahleda,R.,etal.,PhaseI,first-in-humanstudyoffutibatinib,ahighlyselective,,2020.31(10):
21.Mazzaferro,V.,etal.,Derazantinib(ARQ087)inadvancedori,2019.120(2):
22.Javle,M.,etal.,PhaseIISt,2018.36(3):
23.Bahleda,R.,etal.,MulticenterPhaseIStudyofErdafitinib(JNJ-42756493),OralPan-FibroblastGrowthFactorReceptorInhibitor,,2019.25(16):
24.Schuler,M.,etal.,RogaratinibinpatientswithadvancedcancersselectedbyFGFRmRNAexpression:,2019.20(10):
25.Voss,,etal.,APhaseI,Open-Label,Multicenter,Dose-escalationStudyoftheOralSelectiveFGFRInhibitorDebio1347,2019.25(9):
26.Xie,C.,etal.,Preclinicalcharacterizationofanlotinib,ahighlypoten,2018.109(4):
27.GoyalL.,etal.,FOENIX-CCA2:AphaseII,open-label,multicenterstudyoffutibatinibin
patients(pts)withintrahepaticcholangiocarcinoma(iCCA);38(15_suppl):
28.,etal.,AphaseIIIstudyoffutibatinib(TAS-120)versusgemcitabine-cisplatin(gem-cis)chemotherapyasfirst-line(1L)treatmentforpatients(pts)withadvanced(adv)cholangiocarcinoma(CCA)harboringfibroblastgrowthfactorreceptor2(FGFR2)generearrangements(FOENIX-CCA3).JClinOncol2020;38():TPS600.
29.Javle,,etal.,FinalResultsfromaPhaseIIStudyofInfigratinib(BGJ398),anFGFR-selectiveTyrosineKinaseInhibitor,inPatientswithPreviouslyTreatedAdva;39.(3_suppl):
30.,etal.,Infigratinibversusgemcitabinepluscisplatinmulticenter,open-label,randomized,phase3studyinpatientswithadvancedcholangiocarcinomawithFGFR2genefusions/translocations:;37():TPS4155.
31.ParkJO.,afetyoferdafitinibinAsianadvancedcholangiocarcinoma(CCA);37():4117.
未完待续
敬请期待·第五期
版权声明